Rappelons les enjeux majeurs associés à l’implantation cochléaire précoce chez le jeune enfant. La surdité neurosensorielle profonde concerne environ 1 naissance sur 1 000 (données Inserm 2023), et près de 40 % des surdités sévères à profondes sont identifiées avant l’âge d’un an grâce au dépistage néonatal. L’âge moyen du diagnostic est de 3,2 mois[1].
L’implantation précoce repose sur la période de plasticité cérébrale maximale – avant 2 ans – durant laquelle les aires auditives se structurent sous l’effet de la stimulation sonore. Une implantation avant 12 à 18 mois permet ainsi d’obtenir un développement auditif plus proche de celui des enfants normo-entendants, avec un accès accéléré à la détection, la discrimination et la reconnaissance de la parole.
Les bénéfices attendus incluent une acquisition langagière optimisée, une meilleure adaptation aux environnements sonores complexes et une diminution des risques de retards secondaires (langagiers, phonologiques, cognitifs ou attentionnels). C’est dans ce contexte que s’inscrit le parcours de l’enfant N., implanté de manière précoce et suivi selon un protocole structuré.
Cas Clinique
Le protocole établi au CHU de l’hôpital Robert Debré (Paris) prévoit une séquence précise d’étapes pré et post chirurgicales : dépistage, bilan pré-implantation, activation précoce dès J1, réglages rapprochés (J8, M1, M2, M3…), suivi vestibulaire, bilans orthophoniques et consultations ORL. Les enfants sont suivis pendant tout leur parcours jusqu’à l’âge adulte où ils sont ensuite pris en charge par un centre adulte. L’outil APCEI[2] est principalement utilisé pour suivre l’évolution auditive et langagière du jeune enfant implanté, en évaluant l’Acceptation de l’appareil, les Perceptions auditives, la Compréhension du message oral sans lecture labiale, l’Expression orale et l’Intelligibilité & articulation.
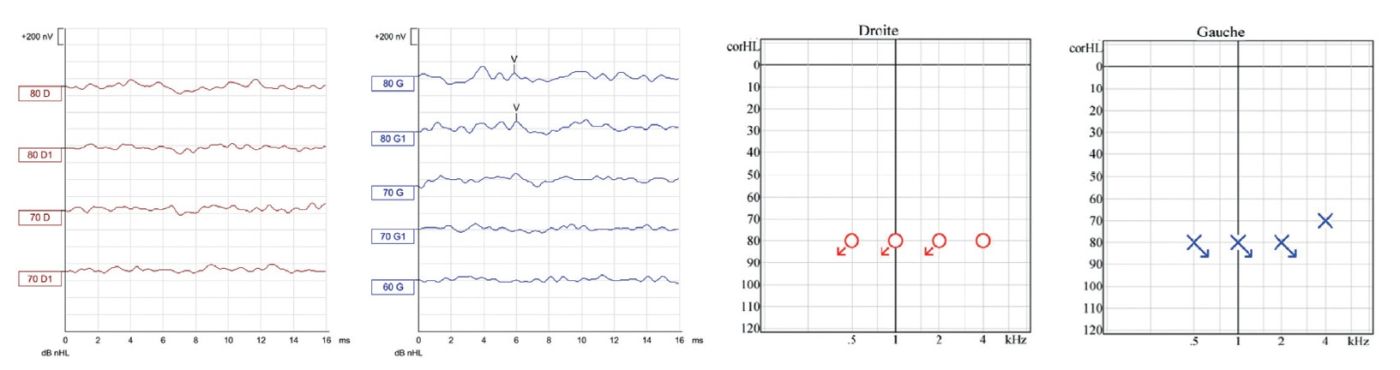
N., ayant eu un dépistage bilatéral non concluant à la naissance (OEA absentes), présente une surdité sévère bilatérale, confirmée à l’âge de 9 mois, après prise en charge d’une otite séro-muqueuse bilatérale. Elle n’a pas d’antécédent médical et les examens étiologiques (CMV, IRM, bilan vestibulaire, ECG) n’identifient pas de cause, orientant vers une surdité d’origine indéterminée. On sait maintenant que sa surdité est d’origine génétique, due à une mutation du gène GATA3 (figure1).
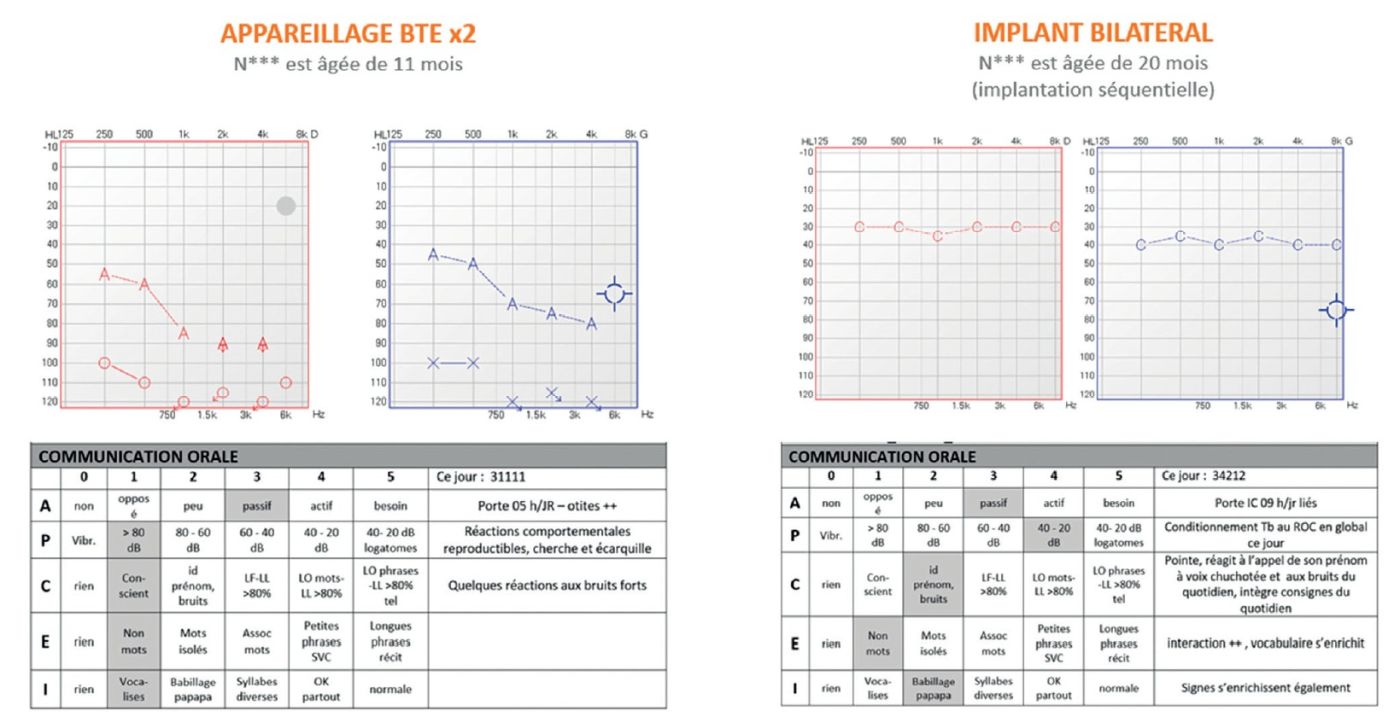
Une amplification bilatérale par aides auditives BTE est donc mise en place afin d’évaluer les bénéfices prothétiques. N. bénéficie d’une implantation cochléaire bilatérale séquentielle : 1er côté à 13 mois et 2ème côté à 15 mois (électrode CI632 Cochlear, processeur CP1000). L’activation précoce à J1 limite le stress parental et assure une mise en stimulation immédiate (figure 2).
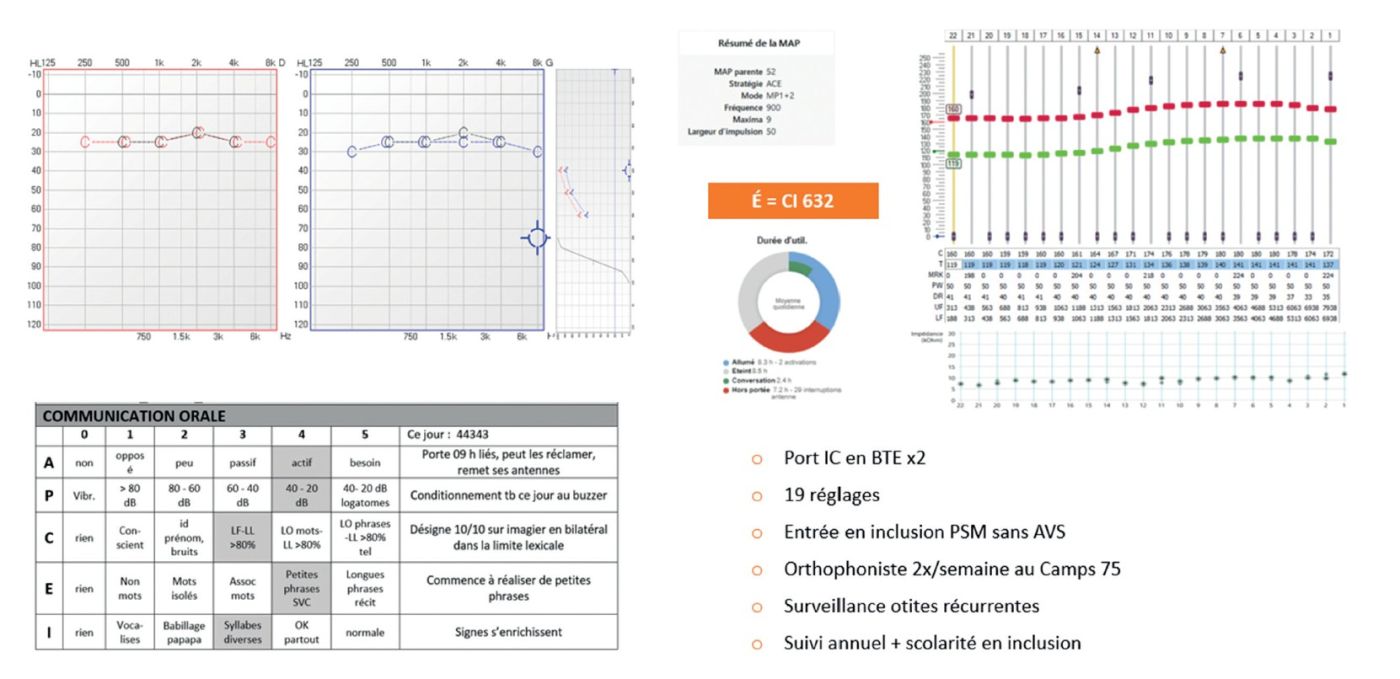
Durant les 24 premiers mois post implantation, N. bénéficie de 19 réglages, de bilans orthophoniques réguliers et d’un suivi ORL rapproché. Les audiogrammes avec implants montrent une progression vers des seuils « micro » (20–30 dB), conformes aux objectifs institutionnels. L’évolution selon l’APCEI atteste d’une amélioration constante des compétences d’expression, de compréhension et d’intelligibilité.
À 3 ans et 1 mois, les mesures audiologiques et le développement langagier témoignent d’une évolution très favorable, permettant une entrée en maternelle en inclusion complète, sans AESH (figure 3).
Pertinence du choix du questionnaire du qualité de vie chez le très jeune enfant
Les travaux menés à l’hôpital Robert-Debré et publiés en 2025[3] ont évalué deux questionnaires de qualité de vie utilisés chez l’enfant implanté cochléaire : le CIQOL-10 Global[4] et le PEACH[5]. Cette étude s’inscrit dans le cadre du registre EPIIC, dont l’objectif était de vérifier l’adhésion aux recommandations d’implantation cochléaire et d’évaluer l’efficacité des implants, notamment par la complétion systématique du CIQOL-10.
Méthodologie
Quarante enfants implantés, âgés de 18 mois à 15 ans et suivis au CHU, ont été inclus afin d’être le plus représentatif de la population pédiatrique implantée. Les parents ont complété les questionnaires CIQOL-10 Global et PEACH, puis en ont évalué la facilité de remplissage et la pertinence clinique sur une échelle visuelle analogique de 0 à 10. Une analyse par tranches d’âge (≤6 ans / >6 ans) a été réalisée pour tenir compte du développement langagier et socio-émotionnel.
Résultats
Le PEACH ressort comme l’outil le plus intuitif : il obtient une note moyenne légèrement supérieure à 9/10 pour la facilité d’utilisation, contre environ 8/10 pour le CIQOL-10. Sa pertinence clinique est également jugée meilleure pour décrire les performances auditives quotidiennes d’après les familles.
Chez les enfants de moins de 6 ans, le CIQOL-10 présente des limites marquées : en moyenne 3 non-réponses sur 10 items, contre 1 sur 13 pour le PEACH. Ces omissions concernent essentiellement des dimensions inadaptées aux très jeunes enfants (estime de soi, évitement social).
Chez les plus de 6 ans, le CIQOL devient progressivement plus exploitable, reflétant un niveau de langage et une maturité sociale qui permet aux parents de mieux évaluer les situations proposées.
Conclusion
L’étude conclut que le PEACH est l’outil le plus adapté pour évaluer la qualité de vie des enfants implantés de moins de 6 ans, grâce à sa pertinence clinique, sa simplicité et son taux de réponses. Le CIQOL peut être utilisé en complément chez les enfants plus âgés, où les différences avec le PEACH deviennent moins marquées. Ces résultats soutiennent l’intégration du PEACH dans les protocoles de suivi pédiatriques, notamment pour les jeunes enfants implantés.
Discussion
Le cas de N. illustre que l’efficacité d’une prise en charge précoce repose sur une organisation institutionnelle structurée, l’utilisation d’outils d’évaluation adaptés à l’âge, ainsi que sur une collaboration étroite et continue entre professionnels.
La confrontation des mesures audiologiques, des observations cliniques et du vécu parental permet d’optimiser les réglages, de détecter rapidement les anomalies éventuelles, de suivre le développement langagier et de soutenir le projet scolaire (inclusion, orientation spécialisée).
Dans ce parcours, l’audioprothésiste assure le suivi fonctionnel quotidien, tandis que l’ORL garantit la sécurité médicale et la cohérence de la prise en charge. Ce cas clinique illustre l’impact positif d’une implantation cochléaire hyper précoce, soutenue par un protocole structuré et une collaboration étroite entre ORL et audioprothésiste. Grâce à cette synergie, N. bénéficie d’un développement langagier optimal et d’une intégration sociale réussie dès l’école maternelle. Les résultats institutionnels réalisés au sein du CHU mettent en avant la pertinence de l’usage combiné de l’APCEI et du PEACH dans le suivi des jeunes enfants implantés.
Nanzeeba-Ibnat-AdobeStock_1468778871-c542.jpg)




